Có 2 lít ddNaCl 0,5M.Khối lượng kim loại và thể tích khí thu đc(dktc)khi đpnc NaCl(hiệu suất điều chế bằng 90%)

Những câu hỏi liên quan
Có 2 lít dung dịch NaCl nồng độ 0,5 mol/l
a, Làm thế nào có thể diều chế Na từ dung dịch NaCl ?
b, Tính lượng kim loại và thể tích khí ( đktc ) điều chế được , nếu hiệu suất quá trình 90%
# Hóa #
Ngòai 3 môn Tóan Văn Anh thì bạn sang H.vn để hỏi nhé!
Đúng 0
Bình luận (0)
Mọi muối clorua điện phân nước đều đc
\(NaCl\rightarrow^{đpn}Na+Cl_2\)
bn tự xử câu sau nha
Đúng 0
Bình luận (0)
Sửa lại điện phân nóng chảy
Mọi muối clorua đều đpnc đc
Đúng 0
Bình luận (0)
Dùng 15,68 lít khí etilec ( đktc) điều chế rượu etylic, hiệu suất pư đạt 90%. A. Tính thể tích rượu etylic thu đc, bt khối lượng riêng của rượu etylic là 0.8 g/ml. B. Dùng toàn bộ rượu etylic thu đx ở trên điều chế axit axetic, tính khối lượng dd axit axetic 5% thu đc
a, \(n_{C_2H_4}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
PT: \(C_2H_4+H_2O\underrightarrow{^{t^o,xt}}C_2H_5OH\)
Theo PT: \(n_{C_2H_5OH\left(LT\right)}=n_{C_2H_4}=0,7\left(mol\right)\)
Mà: H = 90%
\(\Rightarrow n_{C_2H_5OH\left(TT\right)}=0,7.90\%=0,63\left(mol\right)\)
\(\Rightarrow m_{C_2H_5OH\left(TT\right)}=0,63.46=28,98\left(g\right)\)
\(\Rightarrow V_{C_2H_5OH}=\dfrac{28,98}{0,8}=36,225\left(ml\right)\)
b, \(C_2H_5OH+O_2\underrightarrow{^{mengiam}}CH_3COOH+H_2O\)
Theo PT: \(n_{CH_3COOH}=n_{C_2H_5OH}=0,63\left(mol\right)\)
\(\Rightarrow m_{CH_3COOH}=0,63.60=37,8\left(g\right)\)
\(\Rightarrow m_{ddCH_3COOH}=\dfrac{37,8}{5\%}=756\left(g\right)\)
Đúng 1
Bình luận (0)
Hoà tan cùng một lượng kim loại R vào dung dịch HNO3 đặc nóng và vào dung dịch H2SO4 loãng thì thể tích NO2 thu được bằng 3 lần thể tích H2 cùng điều kiện, khối lượng muối sunfat bằng 62,81% khối lượng muối nitrat tạo thành. Mặt khác khi nung cùng một lượng kim loại R như trên thì cần thể tích O2 bằng 22,22% thể tích NO2 ở trên cùng điều kiện thu được chất rắn A. Hoà tan 20,88 gam A vào dung dịch HNO3 20% (lấy dư 25% so vói lượng cần thiết) thu được 0,672 lít khí B (dktc) là một oxit của nitơ Nx...
Đọc tiếp
Hoà tan cùng một lượng kim loại R vào dung dịch HNO3 đặc nóng và vào dung dịch H2SO4 loãng thì thể tích NO2 thu được bằng 3 lần thể tích H2 cùng điều kiện, khối lượng muối sunfat bằng 62,81% khối lượng muối nitrat tạo thành. Mặt khác khi nung cùng một lượng kim loại R như trên thì cần thể tích O2 bằng 22,22% thể tích NO2 ở trên cùng điều kiện thu được chất rắn A. Hoà tan 20,88 gam A vào dung dịch HNO3 20% (lấy dư 25% so vói lượng cần thiết) thu được 0,672 lít khí B (dktc) là một oxit của nitơ NxOy. Khối lượng dung dịch HNO3 đã sử dụng là:
A. 66,15 gam
B. 264,6 gam
C. 330,75 gam
D. 266,4 gam
Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà n N O 2 = 3 n H 2 n ê n n e n h ư ờ n g ( 1 ) = n N O 2 n e n h ư ờ n g ( 2 ) = 2 n H 2
Nên ne nhường(1) =3/2 ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
n e n h ư ờ n g ( 1 ) n e n h ư ờ n g ( 2 ) = n R . h o a t r i 1 n p . h o a t r i 2 = 3 2
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
m R S O 4 = 62 , 81 % m R ( N O 3 ) 2
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là: n NO2= 3nFe=9
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
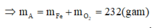
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:
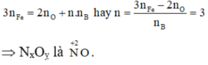
Khi đó:
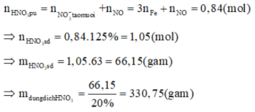
Đúng 0
Bình luận (0)
Hoà tan cùng một lượng kim loại R vào dung dịch HNO3 đặc nóng và vào dung dịch H2SO4 loãng thì thể tích NO2 thu được bằng 3 lần thể tích H2 cùng điều kiện, khối lượng muối sunfat bằng 62,81% khối lượng muối nitrat tạo thành. Mặt khác khi nung cùng một lượng kim loại R như trên thì cần thể tích O2 bằng 22,22% thể tích NO2 ở trên cùng điều kiện thu được chất rắn A. Hoà tan 20,88 gam A vào dung dịch HNO3 20% (lấy dư 25% so vói lượng cần thiết) thu được 0,672 lít khí B (dktc) là một oxit của nitơ Nx...
Đọc tiếp
Hoà tan cùng một lượng kim loại R vào dung dịch HNO3 đặc nóng và vào dung dịch H2SO4 loãng thì thể tích NO2 thu được bằng 3 lần thể tích H2 cùng điều kiện, khối lượng muối sunfat bằng 62,81% khối lượng muối nitrat tạo thành. Mặt khác khi nung cùng một lượng kim loại R như trên thì cần thể tích O2 bằng 22,22% thể tích NO2 ở trên cùng điều kiện thu được chất rắn A. Hoà tan 20,88 gam A vào dung dịch HNO3 20% (lấy dư 25% so vói lượng cần thiết) thu được 0,672 lít khí B (dktc) là một oxit của nitơ NxOy. Khối lượng dung dịch HNO3 đã sử dụng là:
A. 66,15 gam
B. 264,6 gam
C. 330,75 gam
D. 266,4 gam
Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà nên
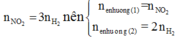
Nên ne nhường(1) = ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
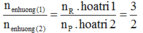
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
![]()
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là:
![]()
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
![]()
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử N + 5 nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:

Þ NxOỵ là .
Khi đó
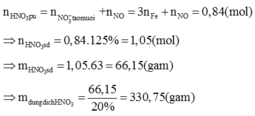
Đúng 0
Bình luận (0)
Điện phân 2 lít dung dịch hỗn hợp gồm NaCl và CuSO4 đến khi H2O bị điện phân ở hai cực thì dừng lại, tại catốt thu 1.28 gam kim loại và anôt thu 0.336 lít khí (ở điều kiện tiêu chuẩn). Coi thể tích dung dịch không đổi thì pH của dung dịch thu được bằng A. 12 B. 13 C. 2 D. 3
Đọc tiếp
Điện phân 2 lít dung dịch hỗn hợp gồm NaCl và CuSO4 đến khi H2O bị điện phân ở hai cực thì dừng lại, tại catốt thu 1.28 gam kim loại và anôt thu 0.336 lít khí (ở điều kiện tiêu chuẩn). Coi thể tích dung dịch không đổi thì pH của dung dịch thu được bằng
A. 12
B. 13
C. 2
D. 3
Có 2 lít dung dịch NaCl nồng độ 0,5 mol/l
a, Làm thế nào có thể diều chế Na từ dung dịch NaCl ?
b, Tính lượng kim loại và thể tích khí ( đktc ) điều chế được , nếu hiệu suất quá trình 90%
a, Có thể điều chế Na kim loại từ dung dịch NaCl bằng cách đun nóng để kết tinh muối NaCl khan, sau đó điện phân NaCl nóng chảy thì thu được Na
b,Phương trình điện phân:
2NaCl \(\rightarrow\) 2Na + Cl2
2mol 2mol 1 mol
Số mol Na = số mol NaCl = 2.0,5 = 1 mol hay 23 gam nếu hiệu suất 100%
\(\frac{23.90}{100}=20,7gam\) nếu hiệu suất 90%
Số mol Cl2 =\(\frac{1}{2}\) số mol NaCl = 0,5
\(\Rightarrow V_{Cl_2}=\frac{11,2.90}{100}=10,08\)( lít )
Đúng 0
Bình luận (0)
a) Điều chế Na từ dung dịch NaCl
- Cô cạn dd NaCl để tạo thành rắn NaCl khan
- Sau đó điện phân nóng chảy NaCl thu được Na
NaCl -đpnc-> Na + 1/2Cl2
b)
nNaCl= 0.5*2=1 mol
nNaCl(pư) = 1*90/100=0.9 mol
NaCl -đpnc-> Na + 1/2Cl2
0.9_________0.9_____0.45
mNa= 0.9*23=20.7g
VCl2= 0.45*22.4=10.08l
Đúng 0
Bình luận (0)
Khử m gam hốn hợp Y gồm \(Fe_2O_3,FeO,Fe_3O_4,CuO\) bằng lượng CO ở nhiệt độ cao. Sau PU thu đc hỗn hợp kim loại R có khối lượng 40g và V lít \(CO_2\) (dktc), Dẫn V lít khí qua đ nước vôi trong dư thì thu đc 30g kết tủa. Viết các PTPU và tính m
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3.........0.3\)
\(CO+O\rightarrow CO_2\)
\(......0.3......0.3\)
\(m_Y=m_R+m_O=40+0.3\cdot16=44.8\left(g\right)\)
Đúng 3
Bình luận (0)
\(Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2\\ FeO + CO \xrightarrow{t^o} Fe + CO_2\\ Fe_3O_4 + 4CO \xrightarrow{t^o} 3Fe + 4H_2O\\ CuO + CO \xrightarrow{t^o} Cu + CO_2\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} = \dfrac{30}{100} = 0,3(mol)\\ CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{CO_2} = 0,3(mol)\\ \Rightarrow m = m_{kim\ loại} + m_{O(oxit)} = 40 + 0,3.16 = 44,8(gam)\)
Đúng 3
Bình luận (0)
Người ta điều chế khí oxi bằng cách nung 19,6 gam KClO3.Tính thể tích khí oxi thu đc , biết hiệu suất p/ứ đạt 80%.
Ta có: \(n_{KClO_3}=\dfrac{19,6}{122,5}=0,16\left(mol\right)\)
PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
____0,16___________0,24 (mol)
Mà: H% = 80%
⇒ nO2 = 0,24.80% = 0,192 (mol)
\(\Rightarrow V_{O_2}=0,192.22,4=4,3008\left(l\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Khi cho cùng một lượng kim loại M vào dung dịch HNO3 đặc nóng dư và dung dịch H2SO4 loãng dư, phản ứng hoàn toàn thì thể tích khí NO2 (sản phẩm khử duy nhất) thu được gấp 3 lần thể tích khí H2 ở cùng điều kiện nhiệt độ và áp suất. Khối lượng muối sunfat thu được bằng 62,81% khối lượng muối nitrat tạo thành. Xác định kim loại M? A. Zn B. Fe C. Mg D. Ca
Đọc tiếp
Khi cho cùng một lượng kim loại M vào dung dịch HNO3 đặc nóng dư và dung dịch H2SO4 loãng dư, phản ứng hoàn toàn thì thể tích khí NO2 (sản phẩm khử duy nhất) thu được gấp 3 lần thể tích khí H2 ở cùng điều kiện nhiệt độ và áp suất. Khối lượng muối sunfat thu được bằng 62,81% khối lượng muối nitrat tạo thành. Xác định kim loại M?
A. Zn
B. Fe
C. Mg
D. Ca
Gọi n, m là hóa trị của R khi tác dụng HNO3 và H2SO4 loãng ( 1≤ m≤ n≤ 3)
Chọn nR= 1 mol
2R + mH2SO4 →R2(SO4)m + mH2↑
1 → 0,5 0,5m
R + 2nHNO3 →R(NO3)n + nNO2 + nH2O
1 1 n
Ta có: n=3.0,5m n=1,5m m=2, n=3 là phù hợp.
Ta có: (R + 96)=(R + 186). 0,6281 R=56 R là Fe.
Đáp án B
Đúng 0
Bình luận (0)



















